- Услуги
- Цена и срок
- О компании
- Контакты
- Способы оплаты
- Гарантии
- Отзывы
- Вакансии
- Блог
- Справочник
- Заказать консультацию
Заказать консультацию
Нормативно-техническая документация при проведении товароведческого анализа
Обеспечить высокое качество медицинской помощи невозможно без разработки требований к качеству медицинских и фармацевтических товаров.
Еще 2000 лет назад Гиппократ в своем труде «О врачебном кабинетеc обратил на это внимание. В нем мы находим описание рабочего места врача, требования к табелю оснащения кабинета (т.е. медицинским и фармацевтическим товарам), его освещенности и др.
На рубеже XIX–XX вв., когда в России приступили к промышленному производству товаров медицинского назначения, были разработаны «Правила об условиях, порядке разрешения и об устройстве фабрик, лабораторий и особых отделений заводов для изготовления сложных фармацевтических препаратовc и первые документы по обеспечению качества медицинских инструментов. В 1925 г. в нашей стране требования к качеству товаров были повышены.
Был организован Комитет по стандартизации, который разрабатывал и утверждал общесоюзные стандарты. А в 1929 г. впервые была установлена уголовная ответственность за несоблюдение обязательных стандартов и выпуск недоброкачественной продукции.
В 1954 г. Комитет по стандартизации был преобразован в Комитет стандартов, мер и измерительных приборов при Совете Министров СССР. В ноябре 1970 г. он был преобразован в Государственный комитет Совета министров СССР по стандартам (Госстандарт СССР).
В 1992 г. — в Государственный комитет Российской Федерации по стандартизации и метрологии (Госстандарт России) и, наконец, в 2004 г. — в Федеральное агентство по техническому регулированию и метрологии.
Это агентство представляет Российскую Федерацию в Международной организации стандартизации (ISO — английская транскрипция, ИСО — русская), которая была создана при ООН в октябре 1946 года. Основной задачей ИСО является разработка международных рекомендаций (стандартов) для содействия международной торговле и научно-техническому прогрессу.
ИСО и ее техническими комитетами, комиссиями, подкомиссиями и группами проделана большая работа по созданию, согласованию и утверждению проектов международных рекомендаций по стандартизации. На протяжении многих лет Россию в ИСО представляли перечисленные выше государственные органы по стандартизации.
Для создания и утверждения необходимых международных стандартов создан ряд комиссий и комитетов: Международная ээкономическая комиссия (IEC — английская транскрипция, МЭК — русская), Европейский комитет нормирования (CEN — английская транскрипция, ЕКН — русская), Европейский комитет электротехнического нормирования (CENELEC — английская транскрипция, ЕКЭН — русская), Европейская организация по контролю качества (ЕОКК), Международный комитет мер и весов (МКМВ), Международная организация законодательной метрологии (МОЗМ) и др.Всеми вышеперечисленными организациями сформирована система управления (менеджмента) качеством товаров, в том числе и медицинского назначения, поступающих на международный и отечественный рынок.
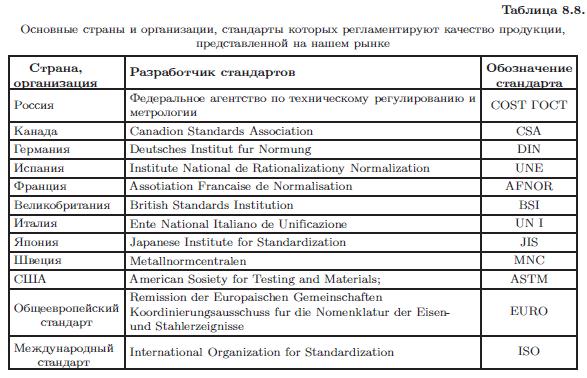
Основные страны и организации, являющиеся членами ИСО, стандарты которых регламентируют качество продукции, представленной на нашем рынке, приведены в табл. 8.8.
Как известно, уровень организации систем управления качеством различных предприятий и выпускаемых ими товаров принято оценивать с помощью утвержденных серий международных стандартов, которые на протяжении уже почти 30 лет действуют во всем мире. Одной из таких серий является ISO 9000 — сертификат качества, появившийся в 1987 году.
За основу данного стандарта были приняты требования, которые военные ведомства США предъявляли к продукции, поставляемой для обороны страны, что говорит о весьма высоком уровне стандарта.
В дальнейшем были разработаны новые модификации этого стандарта, которые включили новые толкования некоторых положений и их корректировки.
Международный стандарт ISO 9000:2000 определял качество — как совокупность характеристик объекта, относящихся к его способности удовлетворять установленные и предполагаемые потребности.
Следовательно, качество медицинских и фармацевтических товаров — это степень их пригодности для удовлетворения потребности пациентов вылечиться.
Требования к качеству товаров устанавливают сначала на этапах его проектирования и разработки, а затем уточняют в процессе выпуска опытных партий.
Высокое качество медицинских и фармацевтических товаров обеспечивают контролем качества исходного сырья, метрологическим контролем оборудования, рабочим и окончательным контролем качества готовой продукции, разработкой требований к условиям хранения и реализации с последующим контролем за соблюдением этих требований.
Перед отпуском товара потребителю производитель оценивает качество товаров по нормам, регламентированным нормативной документацией.
В нормативных документах — устанавливаются правила, общие принципы и их характеристики, касающиеся производства различного вида товаров и требования к свойствам и показателям, обусловливающим их качество.
Как было сказано в гл. 1, требования по технологии производства, качеству, безопасности и эффективности медицинских и фармацевтических товаров отражаются в специальном нормативном документе — техническом регламенте, который утверждается в соответствии с принятым законодательством.
Регламент (от франц. Reglament и лат. reuglo — упорядочивать, регулировать) — правила, устанавливающие, регулирующие порядок и время проведения мероприятий или действий по выпуску готовой продукции и ограничивающие их определенными пределами.
Различают общий технический и специальный технический регламент. Как правило, общий технический регламент касается определенного класса товаров.
Так, межведомственной рабочей группой по техническому регулированию лекарственных средств в 2003 году был разработан проект общего технического регламента «О безопасности лекарственных средствc. Специальный технический регламент на отдельные виды продукции создается производителем (разработчиком) товара.В СССР существовала комплексная система управления качеством продукции (КСУКП). В фармации отраслевая система управления качеством продукции действовала давно, однако особенно серьезно этим вопросом начали заниматься после того, как в 1998 году впервые на отечественном рынке появились фальсифицированные лекарственные препараты.
Цель КСУКП состоит в создании высокого уровня качества продукции при минимальных затратах.
Этого можно добиться для лекарственных препаратов, если внедрить требования GMP и создать новые отечественные лекарственные средства, отвечающие требованиям лучших отечественных и зарубежных образцов.
А также если снять с производства продукцию, не пользующуюся спросом, ускорить внедрение в производство новейших достижений науки и техники.
КСУКП базировалась на стандартах предприятий (СТП), которые разрабатывались в соответствии с государственными и отраслевыми стандартами, учитывали специфику предприятия и были привязаны к конкретным условиям.
Стандарты предприятий строго регламентируют проведение всех организационных, технических и экономических мероприятий по повышению качества продукции.
Комплексность системы проявляется и в том, что она позволяет управлять качеством на всех стадиях жизненного цикла медицинских и фармацевтических товаров, т.е. на стадии разработки, производства, реализации и потребления.
Органы и службы по стандартизации имеют различный уровень в зависимости от назначения стандарта:
- международный уровень (когда стандарт действует между странами участницами);
- национальная стандартизация (стандартизация в одном конкретном государстве):
- государственный уровень
- отраслевой уровень в том или ином секторе экономики (например, на уровне министерств, на уровне ассоциаций, предприятий и др.);
- административно-территориальная стандартизация (края, области, округа).
Работа по стандартизации в России осуществляется руководящим (национальным) органом, рабочими органами и контролирующими организациями.
Надзор за внедрением и соблюдением стандартов для товаров медицинского назначения осуществляется на всех стадиях товародвижения путем:
- регистрации товаров;
- лицензирования различных видов деятельности, связанных с разработкой, производством, продвижением, продажей и использованием товаров;
- подтверждения соответствия товара и его сертификации.
Регистрация товаров медицинского назначения производится по схеме. В результате выдается регистрационное удостоверение — документ, который подтверждает внесение товара в Государственный реестр и разрешает обращение товара на Российском рынке.
Статьи по теме
- Управление комплексом маркетинговых коммуникаций
- Выбор схемы логистики
- Выбор стратегии продвижения нового препарата на рынке
- Создание лекарственного средства
- Разработка бизнес-планов
- Составление планов научных исследований
- Особенности стратегического планирования
- Анализ и интерпретация маркетинговых данных
- Изучение взаимодействия спроса и предложения
Полезные статьи









Узнайте цену услуг:
Узнай цену консультации
"Да забей ты на эти
дипломы и экзамены!”
(дворник Кузьмич)

